近日,我院于妍妍教授课题组成功构建了一种基于级联PMMA芯片平台,实现了从全血样本中高效分离循环肿瘤细胞(CTCs),并精准区分检测上皮和间质表型CTCs。相关成果以“A Cascaded Chip for the High-Purity Capture and Distinguishing Detection of Phenotypic Circulating Tumor Cells in Colon Cancer”为题发表在国际化学权威杂志Analytical Chemistry上(DOI:10.1021/acs.analchem.4c05517)。

循环肿瘤细胞(CTCs)具备完整的细胞结构与功能,携带原发和转移部位的全面基因型,为了解癌症发生、转移过程以及指导癌症治疗提供了重要依据。但CTCs的检测面临诸多挑战。在数十亿血细胞中,CTCs的数量仅为1 - 10个,丰度极低。同时,上皮 - 间质转化(EMT)过程导致其生物特性高度异质,多种表型共存并在转移过程中动态演变。微流控技术虽在液体活检中受到关注,但现有的CTCs捕获方法仍有待完善。

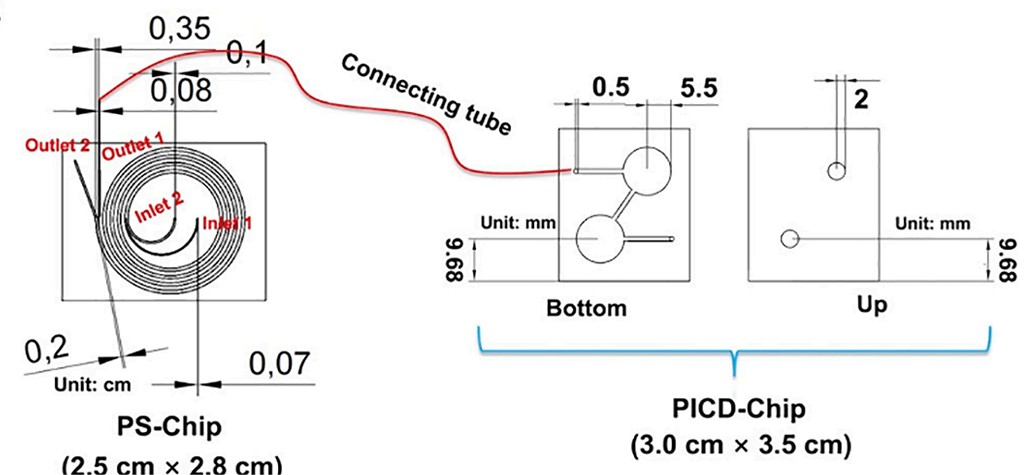
本研究开发的级联芯片由物理分离芯片(PS-Chip)和分区免疫亲和捕获检测芯片(PICD-Chip)串联组成(图1)。PS-Chip 借助迪恩流分馏技术,从全血中对 CTCs 进行聚焦分选,有效去除了血液中约 93.7% 的红细胞和68.4% 的白细胞。PICD-Chip上设有两个独立的腔室,能特异性识别 CTCs 表面的 EpCAM 和Vimentin 蛋白,从而实现对不同表型 CTCs(低至5个/mL)的分区检测。本芯片最终通过收集结肠癌患者的1.0 mL全血样本进行性能验证,明确了 CTCs 数量和表型比例与癌症进展之间的密切关联。
药学院硕士研究生刘婷婷、张雯梦为论文的共同第一作者,于妍妍教授为唯一通讯作者。徐州医科大学药学院为第一作者单位。该研究得到江苏省自然科学基金、徐州市社会发展重点研发计划等项目的资助。
论文链接:https://pubs.acs.org/doi/10.1021/acs.analchem.4c05517



