近日,我院姜力群副教授课题组在期刊《Journal of Controlled Release》发表了题为 “Biomimetic Exosome Harnessing Exosomal Lipidomics and Functional Proteins for PEDF-pDNA Delivery in High Altitude Pulmonary Edema Intervention”的研究论文。该研究创新性地构建了一种基于外泌体脂质组学与功能蛋白仿生的基因递送系统,为高原肺水肿(High Altitude Pulmonary Edema, HAPE)的防治提供了全新的思路。我院2021级药学硕士研究生李慧洋为论文第一作者,姜力群副教授为通讯作者。
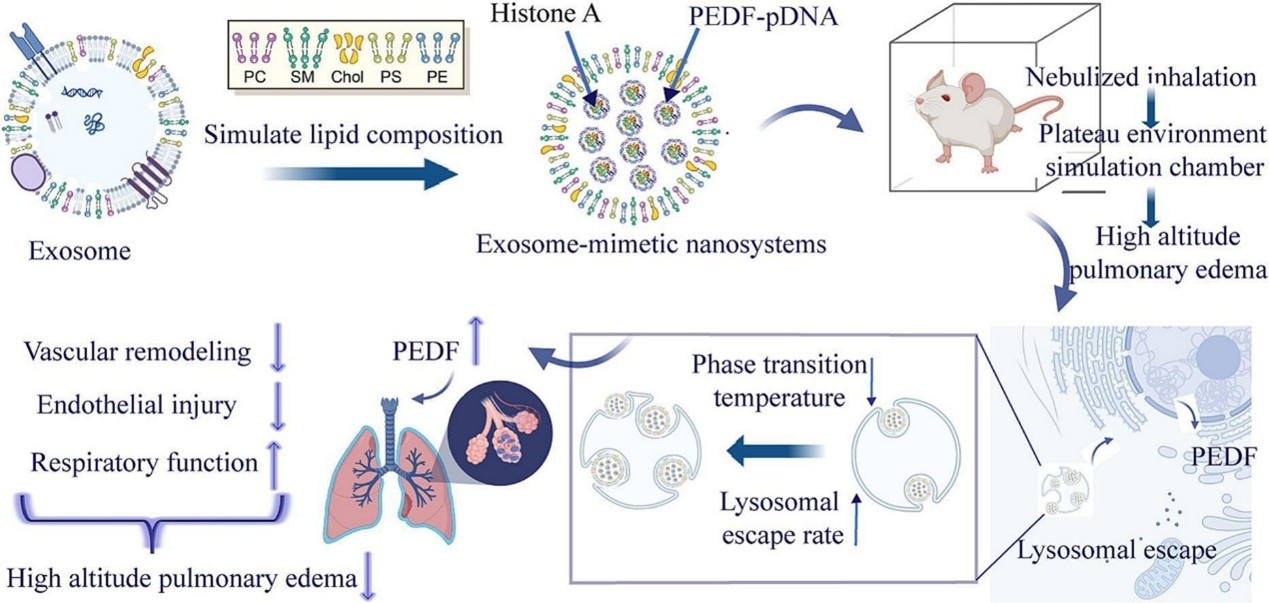
外泌体因其优异的生物相容性和天然的基因递送能力,在基因治疗领域受到广泛关注。然而,目前大多数外泌体仿生纳米囊泡(Exosome-mimetic nanovesicles, EMNs)仍依赖于天然细胞或其提取组分,存在批次差异明显、质量控制困难等问题。针对这一瓶颈,姜力群课题组提出了“成分仿生而非来源仿生”的全新策略,即通过精确模拟外泌体的脂质组成,并引入组蛋白成分,重建外泌体在基因传递中的关键生物功能。研究团队选用鞘磷脂(SM)、磷脂酰胆碱(PC)、磷脂酰丝氨酸(PS)、磷脂酰乙醇胺(PE)及胆固醇作为基础脂质,采用双乳化法制备了携带组蛋白A和PEDF质粒的仿生外泌体(His-pDNA@EMNs)。所得囊泡平均粒径为102 ± 2 nm,Zeta电位为-20 ± 2 mV,并呈现与天然外泌体相似的“杯形”结构。
研究结果表明,与商用转染试剂Lipo6000相比,His-pDNA@EMNs在HUVEC细胞中的PEDF基因转染效率提高了18.74%,且显著降低了细胞毒性,显示出优异的生物安全性和基因递送效率。机理研究进一步发现,仿生脂质组分在递送过程的各个阶段发挥协同作用:PC促进细胞摄取,PE与PS增强溶酶体逃逸,PS与SM的特定组合有助于囊泡跨核膜传递。值得注意的是,该载体能够以完整形态通过局部膜融合机制实现溶酶体逃逸,从而保持基因递送的完整性与高效性。
在细胞和动物模型中,His-pDNA@EMNs均能显著提升PEDF蛋白表达,有效抑制低氧诱导的血管重构与内皮损伤,表现出良好的防治高原肺水肿的潜力。研究不仅验证了利用合成磷脂和组蛋白构建高效仿生基因载体的可行性,也为高原相关疾病的分子干预开辟了新的方向。
本研究得到了国家自然科学基金、国家博士后科学基金及江苏省重点科研项目等的资助。该论文的发表标志着我院在仿生递药系统与高原疾病防治领域的研究取得了新的突破,展示了我院科研团队在创新药物递送与转化医学研究方面的持续实力。
【初审:李桃春;复审:周雪妍;终审:韩爱侠】



