近日,我院张玲教授团队在化学与生物传感领域国际权威期刊《ACS Sensors》(中科院一区Top期刊, IF:9.1)上发表题为“A Near-Infrared Chemiluminescent Probe for Visualizing Norepinephrine in Parkinson's Disease”的研究论文。该研究聚焦帕金森病(PD)发病机制中关键神经递质——去甲肾上腺素(NE)的动态监测难题,创新性设计并合成首个近红外化学发光探针CL-NE,实现了在活体及脑组织中对NE的高灵敏、高选择性实时成像,为揭示PD病理过程中NE动态变化提供了强有力的工具,也为神经系统疾病的早期诊断与药物评价开辟了新路径。
帕金森病作为常见的神经退行性疾病,其病理进程与去甲肾上腺素系统的功能紊乱密切相关。NE在中枢神经系统中参与调控觉醒、运动、认知等多种功能,其水平异常与PD运动障碍、认知衰退等密切相关。目前,NE的检测方法如液相色谱、质谱等存在操作复杂、无法实时原位监测等局限,而传统荧光探针则受限于光漂白、组织穿透性差及背景干扰等问题。因此,开发一种无需外源激发、高信噪比且适用于活体成像的NE检测工具具有重要科学意义与临床价值。
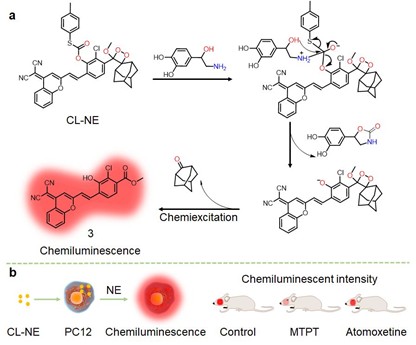
图1. CL-NE检测去甲肾上腺素的机制示意图
研究团队基于1,2-二氧杂环丁烷类化学发光母核,巧妙引入近红外发光团与NE特异性识别基团,成功构建了首例NE响应的近红外化学发光探针CL-NE。该探针在NE存在下,通过亲核取代与分子内环化反应,触发化学发光信号,具有响应迅速(6 min内达峰)、灵敏度高(检测限139 nM)、选择性优异、背景干扰低等优势。得益于其近红外发光特性,CL-NE在活体组织中具有良好的穿透能力。
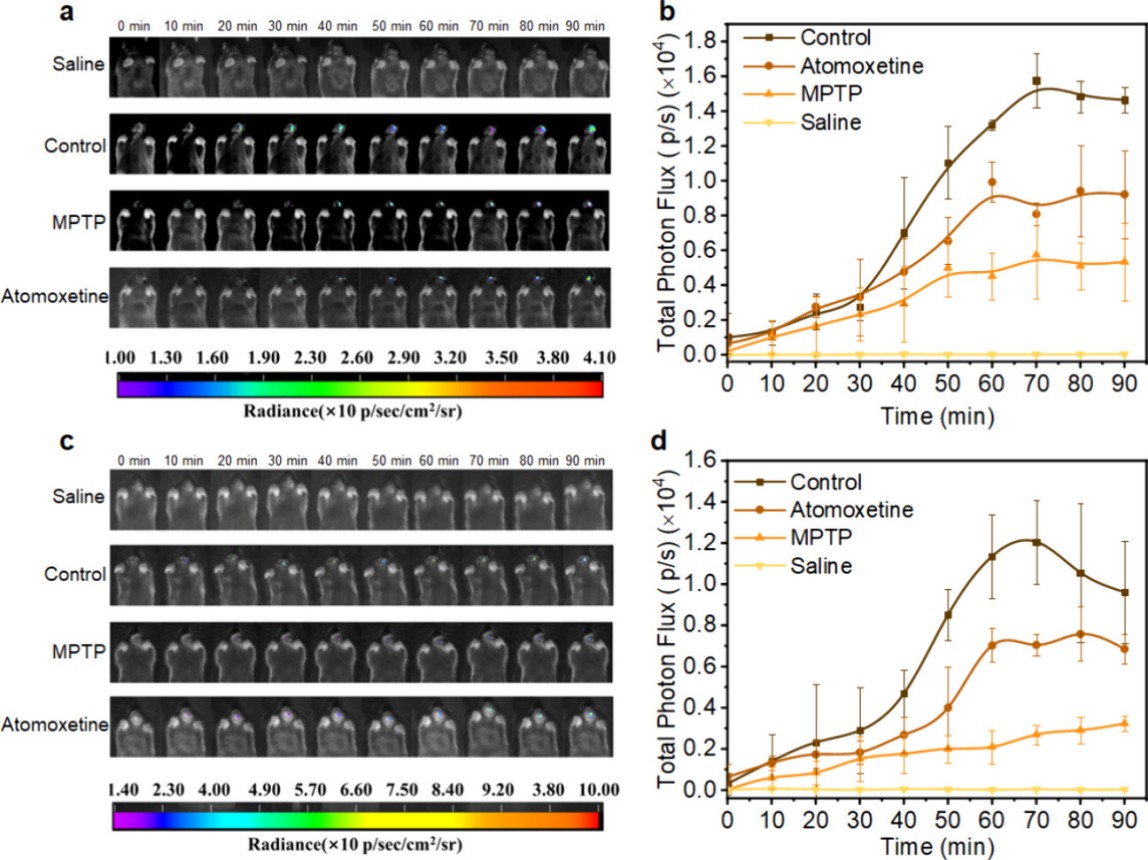
图2. 对照组、帕金森模型组及阿托莫西汀治疗组小鼠纹状体与黑质区域内去甲肾上腺素水平的动态成像
在细胞与动物水平,CL-NE成功实现了对PC12细胞内源NE的实时监测,并能清晰反映MPTP诱导的PD细胞模型中NE水平的下调。进一步,研究团队在MPTP诱导的帕金森病模型小鼠中,在纹状体与黑质区域实现了NE水平的时空动态成像。实验发现PD小鼠上述脑区NE水平显著降低,而经NE再摄取抑制剂阿托莫西汀治疗后,NE水平得到部分恢复,同时伴随运动行为改善与酪氨酸羟化酶表达上调。该结果不仅揭示了NE在PD病理进程中的变化规律,也为通过调节NE系统来干预PD进程提供了直接的影像学证据。
该研究开发的CL-NE探针为在体、实时、可视化研究NE在神经系统疾病中的作用提供了创新工具,不仅有助于深入解析PD等疾病的神经递质调控机制,也为相关疾病的早期诊断、药物筛选与疗效评价提供了新的技术手段。该探针分子设计策略也为开发其他生物标志物的化学发光探针提供了新思路。
我院教师吕壮、研究生李佳怡为论文共同第一作者,薛运生副教授和张玲教授为共同通讯作者,徐州医科大学为唯一完成单位。该研究获得了国家自然科学基金、江苏省高校自然科学基金重大项目、江苏省研究生科研与实践创新计划及徐州医科大学青年基金等项目的支持。
原文链接:https://pubs.acs.org/doi/10.1021/acssensors.5c03087
【初审:李桃春;复审:周雪妍;终审:韩爱侠】



